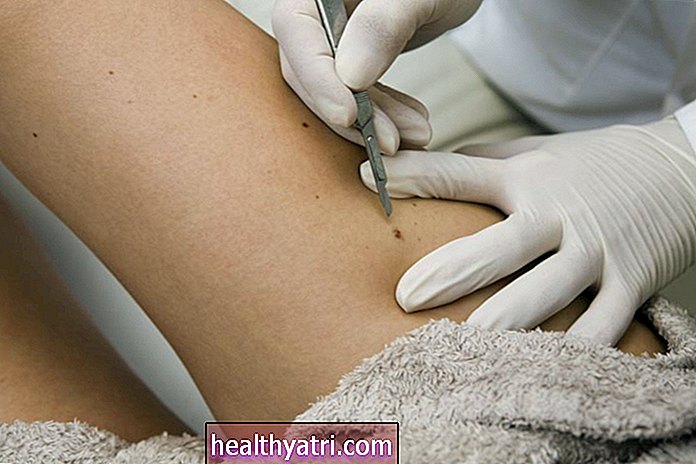
Getty Images
Ključni za poneti
- Uprava za hranu i lijekove (FDA) tražit će od proizvođača cjepiva dva mjeseca sigurnosnih podataka prije nego što odobri cjepivo COVID-19 za upotrebu u široj javnosti.
- FDA vjeruje da će dvomjesečno razdoblje omogućiti dovoljno vremena da se pojave moguće nuspojave ili štetni ishodi potencijalnog cjepiva.
Uprava za hranu i lijekove (FDA) objavila je 6. listopada da će od proizvođača cjepiva COVID-19 tražiti da podijele dva mjeseca sigurnosnih podataka prije nego što odobri cjepivo za upotrebu u široj javnosti. Odluka FDA-e dolazi tamo raste javno nepovjerenje u sigurnost budućeg COVID cjepiva.
Cjepiva protiv COVID-19: Budite u toku s dostupnim cjepivima, tko ih može dobiti i koliko su sigurna.
Novi zahtjevi FDA-e
Prema novim zahtjevima FDA-e, morat će biti dva mjeseca naknadnih podataka o zdravlju dobrovoljaca iz kliničkih ispitivanja nakon što prime druge doze cjepiva. FDA može odlučiti dati proizvođaču cjepiva odobrenje za hitnu uporabu —Oznaka koja omogućava javnu upotrebu proizvoda-ako su ispunjeni novi zahtjevi.
Shobha Swaminathan, dr. Med
Sigurnost je ključna u srcu osiguranja da ljudi vjeruju poslu koji radimo.
- Shobha Swaminathan, dr. MedFDA je u svojim smjernicama objasnila da želi vidjeti podatke iz faze 3 ispitivanja kada su sudionici ispunili puni režim cjepiva i dva mjeseca nakon toga. FDA vjeruje da će ovaj vremenski okvir pružiti "odgovarajuće informacije za procjenu profila koristi i rizika cjepiva".
Prema smjernicama, FDA će proučavati "nuspojave; slučajeve teške bolesti COVID-19 među ispitanicima; i slučajeve COVID-19 koji se javljaju u vremenskom okviru kada su adaptivni (umjesto urođeni) imunološki odgovori na cjepivo bio odgovoran za zaštitni učinak. "
FDA također kaže da mora postojati "dovoljan broj slučajeva ozbiljnog COVID-19 među ispitanicima" kako bi se dokazalo da postoji mali rizik od ljudi koji će razviti ozbiljne komplikacije od cjepiva.
Uz to, FDA očekuje da proizvođači pokažu podatke koji se odnose na određene sindrome - posebno na pojačanu respiratornu bolest povezanu s cjepivom (ERD) iz cjepiva. „Ukupno pet ili više teških slučajeva COVID-19 u skupini koja je primala placebo dovoljno za procjenu podržava li teški slučaj COVID-19 između cjepiva i placebo skupina povoljan profil koristi i rizika ili obratno izaziva zabrinutost. "
Trenutno postoji 11 cjepiva u fazi 3 (završna faza) kliničkih ispitivanja. Međutim, nekoliko ispitivanja koja je provelo nekoliko glavnih farmaceutskih tvrtki nedavno je pauzirano nakon što je barem jedan sudionik studije razvio ozbiljnu, neobjašnjivu bolest.
Slučaj za dvomjesečno čekanje
"Mislim da je sjajno što FDA zahtijeva da imamo dva mjeseca sigurnosnih podataka", stručnjak za zarazne bolesti Shobha Swaminathan, izv. Profesor i glavni istražitelj ispitivanja cjepiva Moderna COVID-19 na Medicinskoj školi Rutgers New Jersey Centar za klinička istraživanja, kaže Verywell. "Sigurnost je ključna u srcu osiguranja da ljudi vjeruju poslu koji radimo."
Swaminathan objašnjava da se najčešće nuspojave od cjepiva javljaju u roku od dva mjeseca. „Većina nuspojava cjepiva, poput vrućice, umora i reakcija na mjestu injekcije, javlja se tijekom prvog tjedna, a složenije se mogu pojaviti tijekom šest tjedana. Zato su minimalna dva mjeseca korisna za otkrivanje onoga što se može dogoditi. "
Shobha Swaminathan, dr. Med
Nemojte prebrzo zaključivati o znanstvenom procesu. Puno je dezinformacija.
- Shobha Swaminathan, dr. MedSwaminathan kaže da vremenski okvir "pokušava uravnotežiti javne potrebe bez ugrožavanja sigurnosti." Nada se da će smjernice FDA-e pomoći u promjeni percepcije javnosti o procesu razvoja cjepiva.
"U javnosti postoji percepcija da se s istraživanjima cjepiva COVID-19 ubrzava prije roka, a neki su ljudi zabrinuti da to dolazi pod cijenu sigurnosnih mjera, što zapravo nije istina", kaže Swaminathan. "FDA donijet će odluku jesu li sigurnosne informacije koje imaju [od istraživača] primjerene. "
Sve u svemu, Swaminathan poziva ljude da vjeruju procesu. „Ne prenagljujte sa zaključcima o znanstvenom procesu. Puno je pogrešnih informacija. "
Što ovo znači za vas
Zahtjev FDA-e za dvomjesečnim kontrolnim podacima nakon što ljudi prime COVID-19 cjepivo trebao bi osigurati da se uoče sve potencijalne nuspojave prije nego što cjepivo postane dostupno široj javnosti. Međutim, postupak u konačnici može potrajati dulje.
Javnost bi se trebala pouzdati u to da je postupak razvoja i odobravanja cjepiva siguran i da FDA neće odobriti cjepivo dok ono ne bude spremno - i sigurno.